항병원생물성 의약품 '아즈트레오남'주사제에서 이상반응 '뇌병증'이 추가되는 사용상의 주의사항 중 경고항이 신설됐다.
식약처는 '아즈트레오남'주사제의 美FDA 안전성 정보와 관련 국내·외 허가 현황, 제출의견 등을 종합 검토한 결과에 따라 이같이 허가사항을 변경지시할 계획이며 이를 25일까지 사전예고한다고 11일 밝혔다.
아즈트레오남 단일제(주사) 허가사항 변경대비표에 따르면 이상반응인 유방통, 칸디다질염, 쇠약, 혼돈,호흡곤란, 흉통, 가슴쓰림 등외에 뇌병증이 추가 신설됐다.
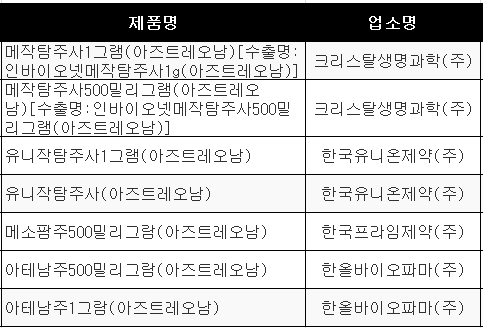
해당품목은 크리스탈생명과학(주) '메작탐주사1g', '메작탐주사500mg', 한국유니온제약(주) '유니작탐주사1g', '유니작탐주사', 한국프라임제약(주) '메소팜주500mg', 한올바이오파마(주) '아테남주500mg','아테남주1g' 등 4개사 7품목이다.
 |
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 심사평가원-원주시노인종합복지관, 아동-어르신 세대 공감 프로젝트 운영 협약 체결
심사평가원-원주시노인종합복지관, 아동-어르신 세대 공감 프로젝트 운영 협약 체결
