국외 시판 후 조사에서 대한약품공업(주) '가르콘주' 등 글루카곤의 이상반응 '괴사유주성홍반'이 추가 보고됐다.
식약처는 美FDA의 '글루카곤'성분제제 관련 안전성 정보에 대한 검토결과에 따라 허가사항 변경안을 마련했으며 해당 사유 및 근거자료를 오는 5월1일까지 제출해 줄 것을 주문했다.
이번에 신설되는 사용상의 주의사항에 따르면‘괴사유주성홍반' 사례는 지속적으로 글루카곤을 주입한 환자에서 국외 시판 후 보고됐다.
또‘괴사유주성홍반(NME)은 글루카곤종(글루카곤 생성종양)과 흔히 관련된 피부발진이며, 비늘모양, 소양홍반성판, 물집, 짓무름이 특징이며 시판 후 지속적인 글루카곤 주입 후에 보고됐다.
괴사유주성홍반 병변은 얼굴, 서혜부, 회음, 다리에 나타날 수 있으며 이보다 더 광범위할 수 있다. 보고된 사례에서 괴사유주성홍반은 글루카곤 중단시 해소되었으며 코르티코스테로이드 투여는 효과적이지 않았다. 괴사유주성홍반 발생 시 지속적인 글루카곤 주입의 유익성이 위험성보다 큰지 고려해야 한다는 일반적 주의사항이 추가됐다.
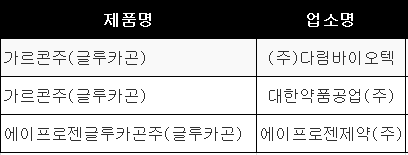
해당품목은 대한약품공업(주) '가르콘주', (주)다림바이오텍, '가르콘주', 에이프로젠제약(주) '에이프로젠글루카곤주' 등 3품목이다.
 |
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
