환인제약(주) 항경련제 '환인히단토인정'등 '페니토인제제' 4품목에서 서맥 및 심정지 이상사례가 추가 보고됐다.
식약처는 美FDA의 '페니토인'성분제제 관련 안전성 정보에 대한 검토결과에 따라 허가사항 변경(안)을 마련했으며 검토의견 및 해당 사유, 근거자료를 6월14일까지 제출해 줄것을 주문했다.
페니토인 허가사항 변경안에 따르면 이 약 투여받은 환자에게서 서맥 및 심정지 사례가 보고됐다. 이 두 이상반응 모두 권장된 용량 투여시 발생했고 페니토인 독성과 연관성이 있었다.
대부분의 심정지 사례는 기저 심장질환이 있는 환자에게서 발생했다.
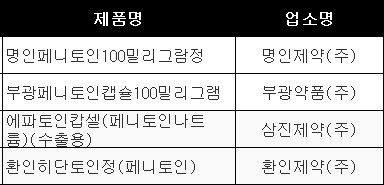
해당제품은 환인제약(주) '환인히단토인정', 삼진제약(주) '에파토인캅셀', 부광약품(주) '부광페니토인캡슐100mg', 명인제약(주) '명인페니토인100mg' 등 4품목이다.
 |
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
