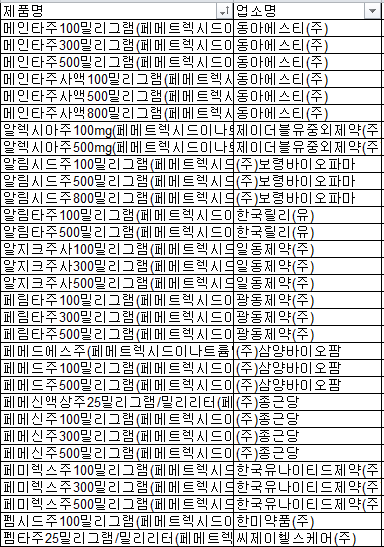
동아에스티(주) '메인타주100mg' 등 페메트렉시드 성분제제 33품목의 국외 시판후 조사에서 이상반응 '급성 박테리아 피부-피하염', '가성 봉와직염 및 피부염', '과다색소침착'이 보고됐다.
식약처는 이같은 '페메트렉시드'성분제제의 유럽 집행위원회(EC) 안전성 정보와 관련 국내 허가사항 변경지시할 계획이며 이를 10월1일까지 사전예고한다고 밝혔다.
페메트렉시드 성분제제(알림타주 500mg 기준)허가사항 변경지시(안)에 따르면 국외 시판후 조사에서 '과다색소침착'이 흔하게 보고됐다.
또 주로 하지의 홍반 부종이 빈도불명으로 보고됐으며 진피, 피하 조직의 감염성 및 비감염성 질환이 빈도불명으로 추가됐다.(예, 급성 박테리아 피부-피하염, 가성 봉와직염 및 피부염)
 |
 |
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
