 |
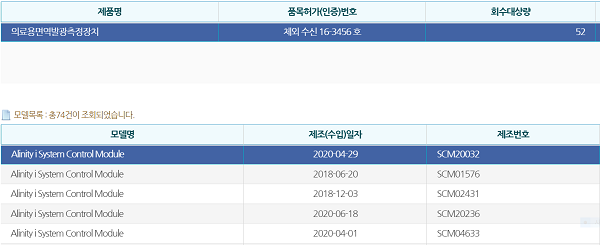
| ▲회수대상제품 |
식약처는 서울시 강남구 소재 한국애보트(유)의 '의료용면역발광측정장치(체외 수신 16-3456호)' 52량을 회수 조치했다.
9일 식약처에 따르면 2020년12월24일 회수계획 202000119996호를 통해 54대의 장비 사용 고객에게 SW update 계획을 통지했다. 해당 회수 계획 통지만 전달 완료후 SW update를 실시하기 위해 추가 회수계획을 신고했다. 애보트는 Alinity ci-series Software version 3.1.2 및 그 이전 버전에서 잠재적 성능 문제를 확인했기 때문이다. 애보트는 이런 문제 해결을 위한 Alinity ci-series Software version 3.2.0을 배포했다.
version 3.2.0에 따르면 1. 특수한 상황에서, 임상화학 광도계 검사시 사용자 정의된 희석 프로토콜을 삭제하면, 해당 검사에 대한 다른 사용자 정의된 프로토콜 수행시 잘못된 희석이 수행될 수 있다. 2. 피펫터 진단 절차 4102 Sample Pipettor Calibration(c-series)가 검체 위치잡이 캘리브레이션 목표물을 놓쳐 부정확한 캘리브레이션 값으로 캘리브레이션을 통과시킬 수 있다. 3. 생물학적 위험, 화학물질 위해 및 가동부(moving parts)와 관련된 주의사항이 Fluidics-Wash 진단 절차 1250 Vacuum Diagnostic (i-series)에 기재되어 있지 않다 등이다.
 |
회수방법은 자사 직원이 SW update하며 소비자는 "소프트웨어 버전 3.2.0이 설치될 때까지 상기 첨부 A에서 요하는 필수 조치에 따라 줄 것"을 주문하고 "애보트 담당자가 Alinity ci-series 소프트웨어 버전 3.2.0.으로의 필수 업그레이드를 진행할 날짜를 조정해드릴 것이다. 만일 상기 제품을 다른 검사실에 전달했다면, 해당 검사실에 이번 제품 시정사항을 고지하고, 본 안내서의 사본을 전달해 달라"며 "첨부된 '애보트 고객 응답서 양식'을 완료해 줄 것과 안내서를 귀 검사실 기록으로 보관할 것"을 요청했다.
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 심사평가원-원주시노인종합복지관, 아동-어르신 세대 공감 프로젝트 운영 협약 체결
심사평가원-원주시노인종합복지관, 아동-어르신 세대 공감 프로젝트 운영 협약 체결
