의약품·의약외품 허가심사 결과 공개 현황 안내
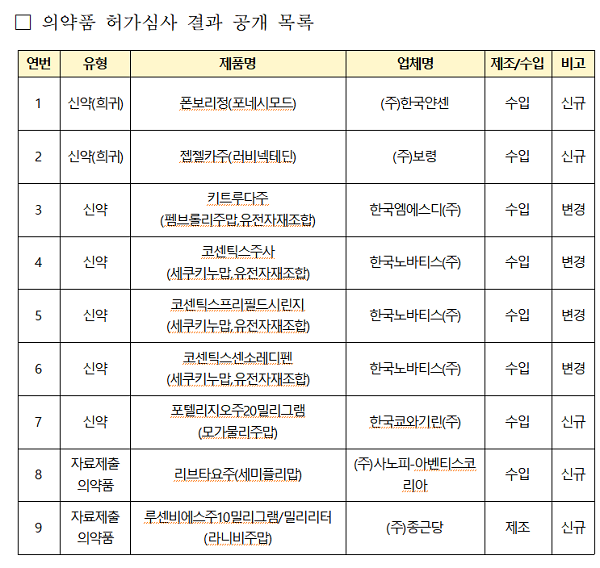 |
식품의약품안전처(처장 오유경)는 의약품과 의약외품 허가심사에 대한 투명성, 일관성, 신뢰성을 강화하기 위해 지난 11월에 의약품 9개, 의약외품 1개 총 10개 품목(신규허가 6개, 변경허가 4개)의 허가심사 결과(허가보고서)를 순차적으로 공개했다.
공개 근거는 '약사법'제88조의2, '의약품 등의 안전에 관한 규칙'(총리령) 제102조의8이며 공개 대상은 ▲신약 ▲자료제출의약품 ▲안전성·유효성 심사대상 의약외품이다.
이번에 허가보고서가 공개된 대표적인 의약품은 ▲피부 T-세포 림프종 치료 신약 ‘포텔리지오주20mg(모가물리주맙)’[한국쿄와기린㈜]과 ▲황반변성 치료제인 ‘라니비주맙’ 제제에 대해 국내에서 두 번째로 개발된 동등생물의약품(바이오시밀러)인 ‘루센비에스주10mg/ml(라니비주맙)’[㈜종근당]▲폰보리정(포네시모드)[(주)한국얀센]▲젭젤카주(러비넥테딘)[(주)보령]▲키트루다주(펨브롤리주맙,유전자재조합)[한국엠에스디(주)]▲코센틱스주사(세쿠키누맙,유전자재조합)[한국노바티스(주)]▲코센틱스프리필드시린지(세쿠키누맙,유전자재조합)[한국노바티스(주)]▲코센틱스센소레디펜(세쿠키누맙,유전자재조합)[한국노바티스(주)]▲리브타요주(세미플리맙)(주)사노피-아벤티스코리아 등이다.
앞서 국내 첫 번째 개발 바이오시밀러 품목은 삼성바이오에피스㈜의 ‘아멜리부주10mg/ml(라니비주맙, 유전자재조합)다.
식약처는 앞으로도 의약품과 의약외품의 허가심사 결과를 공개하고, 매월 공개 목록을 제공함으로써 제약업계의 제품 연구·개발에 도움이 될 수 있도록 노력하겠다고 밝혔다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
반복해서 떠오르는 생각(강박사고)이 일상을 방해한다면(?)
