 |
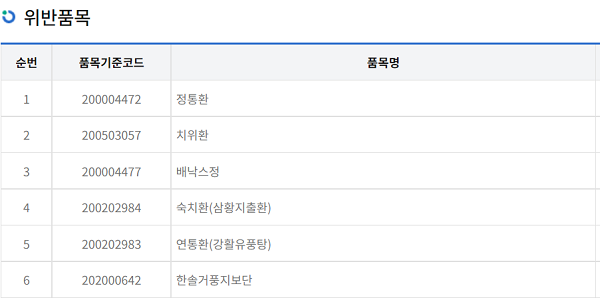
식약처는 제조업 허가 등 위반, 생산 관리 의무 위반 혐의 충북 음성군 소재 한솔신약(주)의 '정통환', '치위환', '배낙스정', '숙취환', '연통환', '한솔거풍지본단'에 대해 제조업무정지 8개월15일의 행정처분을 내렸다. 처분기간은 2022년6월2일~2023년2.16일까지다.
다만 2022년6월2일자 의약품 잠정 제조 판매 중지 명령을 받고 잠정 조치 진행중인 품목에 대해 잠정 조치 기간을 행정처분 기간에 산입해 처분됐다.
29일 식약처에 따르면 한솔신약(주)는 '정통환', '치위환', '배낙스정', '숙취환', '연통환', '한솔거풍지본단' 등 6품목을 제조함에 있어 '주성분 및 부형제 분량, 제조법(전분을 이용해 전분풀 생산후 투여) 등을 임의 변경했음에도 변경허가 또는 변경신고를 신청하지 않은 사실이 있다. 또 '정통환', '치위환', '배낙스정', '숙취환', '연통환', '한솔거풍지본단' 등 6품목을 제조함에 있어 '주성분 및 부형제 분량, 제조법(전분을 이용해 전분풀 생산후 투여) 등을 임의 변경했음에도 제조지시 및 기록서에는 허가 받은 사항에 따라 제조한 것처럼 원료 및 중량을 거짓 작성한 사실이 있다.
또한 '정통환', '치위환', '배낙스정', '숙취환', '연통환', '한솔거풍지본단' 등 6품목에 대해 원료약품 및 그 분량의 변경시 사전에 변경신청, 변경사항에 대한 평가 및 승인 등의 절차를 따라야 함에도 '주성분 및 부형제 분량, 제조법(전분을 이용해 전분풀 생산후 투여) 등을 임의 변경함에 있어 변경관리를 실시하지 않은 사실이 있어 약사법 제31조제1항, 제38조제1항, 의약품 등의 안전에 관한 규칙 제8조제1항, 제48조제9호 가목, 약사법 제76조, 의약품 등의 안전에 관한 규칙 제95조를 위반한 혐의다.
이인선 기자 dailymedipharmn@gmail.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 동국제약, ‘마이핏S 혈당&핑크핏 다이어트’ 엠버서더 ‘핑크어트’ 모집
동국제약, ‘마이핏S 혈당&핑크핏 다이어트’ 엠버서더 ‘핑크어트’ 모집
