국내 글로벌 가이드라인에 발맞춘 최신·최적 치료 가능해져
3상 임상 중추신경계 전이 동반 환자 무진행생존기간 연장 확인 유일한 폐암 표적항암제
지리한 약가협상의 진통끝에 급여가 인정된 아스트라제네카의 비소세포폐암치료제 '타그리소'에 대한 환자의 약값 부담이 月 640만원에서 34만원으로 대폭 줄어든다.
앞서 보험 적용 전에는 폐암환자들이 월 1260만원의 약값 부담을 감수해야만 했다.
 |
한국아스트라제네카는 13일 더플라자호텔에서 세계 최초 T790M 변이 양성 국소 진행성 또는 전이성 비소세포폐암 치료제, ‘타그리소(성분명 오시머티닙)’의 보험 급여 출시를 기념하는 기자간담회를 개최했다.
‘타그리소, 한국 폐암 내성 치료의 새로운 시작’이라는 주제로 진행된 이번 간담회에서는 서울성모병원 종양내과 강진형 교수가 대규모 글로벌 임상 데이터로 확인된 타그리소의 임상적 유용성을, 연세암병원 종양내과 김혜련 교수가 중추신경계 전이 동반 환자들을 대상으로 한 타그리소의 하위 분석 연구 결과 및 타그리소 치료 환자 사례를 소개했다.
타그리소는 EGFR-TKI 치료 경험이 있는 T790M변이 양성 비소세포폐암 환자들을 대상으로 진행된 3상 임상연구 AURA3에서 무진행생존기간 중간값(median PFS by investigator assessed)이 10.1개월인 것을 확인했다.
이는 기존 표준요법인 백금기반 이중 항암화학요법군의 4.4개월 대비 2배 이상 연장된 결과이다.
객관적 반응률(Confirmed ORR) 역시 백금기반 이중 항암화학요법군은 31%인 것에 비해 타그리소 치료군은 71%로 높았다.
이를 바탕으로 미국종합암네트워크(NCCN; National Comprehensive Cancer Network)는 올해 EGFR T790M 변이 양성 비소세포폐암 환자의 치료를 위한 타그리소의 권고 수준을 기존 Category 2A에서 가장 높은 권고 등급인 Category 1으로 상향 조정했다.
미국종합암네트워크의 가이드라인에서 권고되는 3세대 EGFR-TKI은 타그리소가 유일하다는 회사 측 설명이다.
또한 타그리소는 3상 임상시험을 통해 뇌 전이 환자에서의 효과를 보인 최초의 표적치료제이다.
아스트라제네카는 "AURA3 하위 분석 결과, 연구에 참여한 뇌 전이 폐암 환자 중 타그리소 치료군의 무진행생존기간 중간값은 11.7개월로, 백금기반 이중 항암화학요법군의 5.6개월에 비해 2배 이상 연장된 것으로 나타났다"고 설명했다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

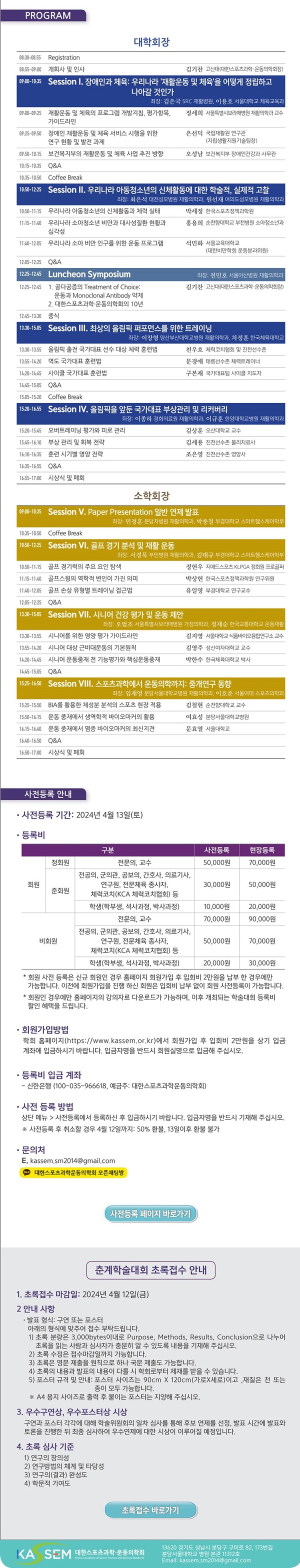 대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
