렘데시비르 3건-옥시크로린정·칼레트라정, 할록신정 각 1건 등 총 5건 임상종료
 |
 |
 |
 |
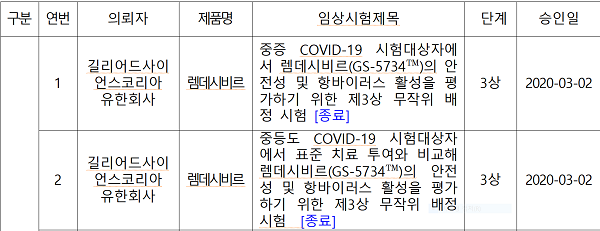
지난 6월 26일 이후 이미 승인된 카모스타트 성분약 이용해 개발 중인 크리스탈지노믹스 'CG-CAM20'와 대웅제약의 'DWJ1248정'이 추가 승인되고 렘데시비르 3건 및 옥시크로린정·칼레트라정, 할록신정 각 1건 등 총 5건이 임상종료된 것으로 나타났다.
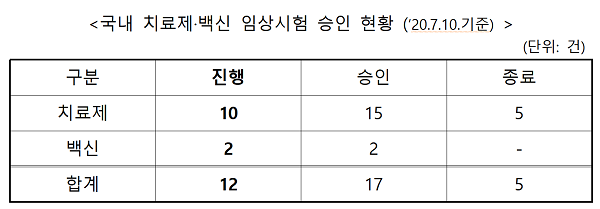
10일 식품의약품안전처(이의경 처장)의 코로나19 치료제·백신의 임상시험 및 허가·심사 현황에 따르면 현재 국내에서 코로나19 관련 진행 중인 임상시험은 치료제 10건, 백신 2건 등 총 12건이다. 지난 6월 26일 발표 이후 2건의 임상시험이 추가로 승인됐으며 5건의 임상시험이 종료됐다.
추가로 승인된 2건은 약물 재창출을 통해 이미 허가된 카모스타트 성분약을 이용해 개발 중인 'CG-CAM20(크리스탈지노믹스)' 및 'DWJ1248정(대웅제약)'이다. 카모스타트는 만성 췌장염 및 역류성 식도염 치료를 위해 사용하는 의약품으로, 세포 단계 시험에서 코로나19 바이러스의 활성을 억제했고, 바이러스가 감염된 마우스(쥐)에서 생존율 개선 효과를 나타냈다.
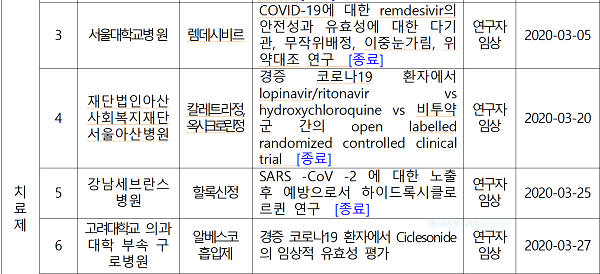
식약처는 "미국, 영국, 독일 등 5개국에서 카모스타트를 이용한 임상시험이 진행되고 있다"며 "종료된 5건의 임상시험은 렘데시비르 3건 및 옥시크로린정·칼레트라정, 할록신정 각 1건이다. 렘데시비르는 계획대로 임상시험이 완료됐으며, 옥시크로린정(히드록시클로르퀸)·칼레트라정 비교임상 및 할록신정(히드록시클로르퀸) 임상의 경우, 히드록시클로로퀸의 코로나19 관련 치료적 유익성이 인정되지 않는다는 해외 연구 결과 등에 따라 종료됐다"고 설명했다.
백신은 2건 모두 초기 단계(1상~2상)에 있으며, 이중 국내개발 백신으로는 GX-19(1/2상, 제넥신)이 있다.
치료제·백신 임상시험 신청 현황에 따르면 현재 임상시험 계획을 심사 중인 코로나19 치료제·백신은 5개이며, 신청을 위해 사전상담이 진행 중인 의약품은 33개다.
심사 중인 5개 제품은 모두 국내 개발 치료제로, 신약 항체치료제가 1개, 약물재창출 치료제가 4개다. 사전상담은 혈장분획치료제 등 치료제 23개 제품, 백신 10개 제품이 진행 중에 있으며, 지역적으로는 국내개발이 27개로 국외개발보다 많다. 이중 혈장분획치료제 등 일부 제품은 조만간 임상시험 승인을 신청할 것으로 예상된다.
치료제·백신 등 관련 국내외 정보에 따르면 최근 국내외에서 공개되고 있는 칼레트라의 치료정보와 관련 영국 및 국제보건기구(WHO) 임상시험 자료를 분석한 결과, 코로나19 입원 환자의 사망률 개선에 대한 효과 부족으로, ‘칼레트라’에 대한 임상시험 중단을 각각 발표했다.
 |
국내에서는 칼레트라와 히드록시클로르퀸을 비교하는 1건의 연구자 임상시험이 승인됐으나, 히드록시클로르퀸의 치료적 유익성이 인정되지 않는 이유로 종료됐다.
식약처는 "영국과 WHO에서는 칼레트라에 대해 사망률 개선을 목표로 계획한 임상시험에서 개선 효과가 부족하다고 판단한 것으로, 향후 지속적으로 국외 관련 정보를 수집 관찰해 나가겠다"고 밝혔다.
현재 전 세계적으로 개발되고 있는 코로나19 백신의 종류는 ▶바이러스벡터 백신=바이러스 항원 유전자를 다른 바이러스에 넣어 투여(영국 A사 3상) ▶불활화 백신=바이러스를 사멸시켜 항원으로 사용(중국 S사 3상) ▶DNA 백신=바이러스 항원을 발현시킬 수 있는 DNA를 투여(국내 G사 1/2상) ▶RNA 백신=바이러스 항원 유전자를 RNA 형태로 투여(미국 M사 2상) ▶재조합 백신=바이러스 항원 단백질을 유전자재조합 기술로 만들어 투여(미국 N사 1/2상) ▶바이러스 유사입자 백신=바이러스 항원 단백질을 바이러스와 유사한 입자 모양으로만들어 투여(캐나다 M사 1상) 등이다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

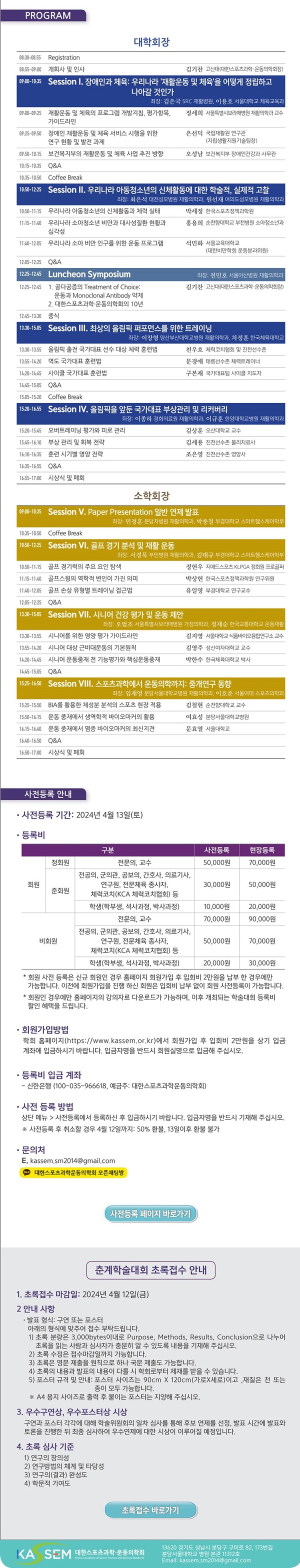 대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
