정식허가 신청제품, 유전자진단시약 9개-항원진단시약 2개-항체진단시약 7개
임상적 성능시험계획 승인 받은 14개 제품, 성능시험 중
시중 사용 코로나19 진단시약 총 16개 제품...수출용 허가 166개 제품
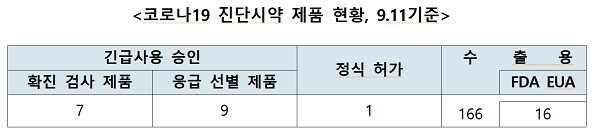 |
현재 코로나19 진단 등을 위해 국내 사용되는 진단시약은 총 16개 제품이며 수출용으로는 166개 제품이 허가받은 것으로 나타났다. 또 18개의 코로나19 진단시약 제품이 정식허가를 신청했고, 임상적 성능시험계획 승인을 받은 14개 제품이 성능시험 중인 것으로 확인됐다.
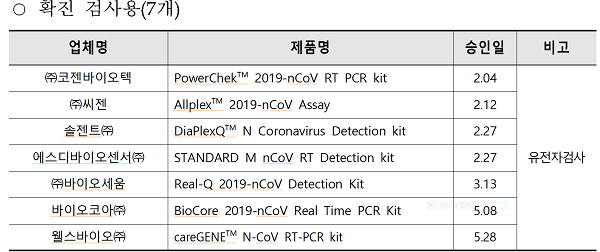
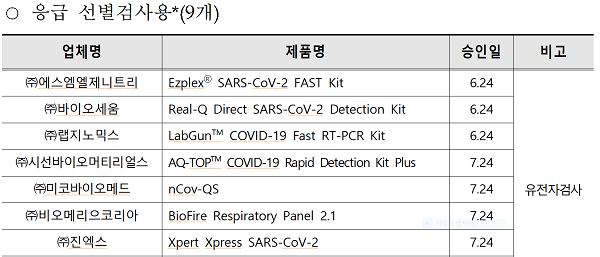
15일 식약처에 따르면 국내 사용이 가능한 제품은 ▲확진 검사용 긴급사용승인 제품 7개 ▲응급 선별용 긴급사용승인 제품 9개 ▲정식허가 제품 1개로 총 16개 제품이 있다.
정식허가 1개 제품은 지난 2월27일 ‘에스디바이오센서㈜’에서 확진검사용 긴급 사용승인 받고 8월31일 정식허가받았다. 수출용으로는 166개 제품이 허가됐으며 그 중 16개 제품이 FDA EUA(긴급사용승인) 제품으로 등록되어 있다.
식약처는 "국내 방역에서 사용 중인 긴급사용 승인된 코로나19 진단시약은 ‘분자진단(RT-PCR) 방식’을 사용하는 유전자 진단시약 제품으로, 사용목적에 따라 확진 검사용과 응급 선별 검사용으로 구분된다"며 "‘확진검사 제품’은 코로나19 감염자의 확진을 목적으로 6시간 이내 결과를 확인해 진단할 수 있다. ‘응급 선별검사 제품’은 1시간 이내 결과를 확인할 수 있는 제품으로, 긴급한 수술이 필요한 환자 등 중증응급환자를 대상으로 빠르게 코로나19 음성을 확인하는 목적으로 사용하고 있다"고 설명했다. 다만, 검사 결과 양성인 경우 ‘확진 검사 제품’으로 재검사해 확진여부를 판단하도록 하고 있다.
식약처는 현재, 유전자 진단시약(RT-PCR) 및 면역검사(항원검사, 항체검사) 등 총 18개의 코로나19 진단시약 제품이 임상적 성능시험을 거쳐 정식허가를 신청했고, 임상적 성능시험계획 승인을 받은 14개 제품이 성능시험 중에 있다고 밝혔다.
정식허가 신청제품 현황은 유전자진단시약 9개, 항원진단시약 2개, 항체진단시약 7개이다.
한편 코로나19 진단시약은 검체 내의 바이러스 유무를 확인하는 ‘유전자 진단시약(RT-PCR)’, ‘항원진단시약’과 검체 내의 바이러스에 대한 항체 유무를 확인하는 ‘항체진단시약’ 등 3종류가 있다.
‘유전자 진단시약’은 환자검체 내의 바이러스 유전자를 증폭하는 ‘분자진단(RT-PCR) 방식으로, 바이러스 유무를 확인해 감염 여부를 진단하며 이 방식은 과학적으로 가장 정확도가 높아, 코로나19 확진용으로 사용하고 있다.
 |
 |
 |
 |
분자진단은 비인두 및 구인두 가검물 등 환자 검체에 포함된 미량의 바이러스 유전자를 분리하고 이를 증폭해 바이러스 유무를 확인하는 방법이다.
‘항원 진단시약’은 바이러스의 특정 단백질을 인식하여 검체내의 바이러스 유무로 감염 여부를 확인한다. 다만, 비인두‧구인두 등 검체를 그대로 사용해 바이러스가 미량인 경우는 검사 결과에 영향을 줄 수 있다. ‘항체 진단시약’은 바이러스 감염에 대한 면역반응으로 만들어진 항체의 생성 유무를 확인하는 제품으로, 항체가 생성되기 이전인 초기 감염단계에는 음성으로 진단될 수 있고 검사 당시의 검체 내 바이러스 유무를 직접적으로 확인하기에는 어려움이 있다.
한편 국내 방역에 사용 중인 코로나19 진단시약의 1일 최대 생산량은 약 16만명분이고, 현재까지 359만명분을 생산, 이중 329만명분이 공급됐고(9월11일 기준) 지금까지 총 212만건의 검사(질병관리청 통계)를 진행했다. 현재 확보된 재고 약 30만명분은 최근 1일 평균 검사량 1.5만명분을 감안할때 약 20일 간 의료현장에 공급할 수 있는 물량으로 안정적인 수급을 이어가고 있다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
