 |
식약처는 서울시 서대문구 소재 지멘스헬시니어스(주)의 '종양표지자면역검사시약(체외 수허 12-1615호)' 21량에 대해 회수조치했다.
2월1일 식약처에 따르면 지멘스헬시니어스(주)는 '종양표지자면역검사시약체외(수허 12-1615호)' 21량에 대해 영업자(자발적) 회수보고이며 국내에 발생하지 않은 문제를 예방하기 위한 안내문 전달 및 교환 조치다.
고객 안내문의 자료(Table 1)에 기재된 칼리브레이터 비율이 정의된 사양의 범위를 벗어나 유효하지 않은 칼리브레이션이 발생할 가능성이 있다. 유효하지 않은 칼리브레이션은 고객이 fPSA 결과를 보고하지 못하게 한다. 이 문제는 간헐적으로 발생하며 일부 고객은 24로 끝나는 Atellica IM fPSA 칼리브레이터 키트 로트와 25로 끝나는 ADVIA Centaur fPSA 칼리브레이터 키트 로트에서 이 문제를 경험할 수 있다. 유효한 칼리브레이션이 이루어지고 정도관리(QC)가 정의된 범위를 충족하는 경우 환자 결과는 정확한 것으로 간주되며 보고할 수 있다. 자사는 상기 사유로 인해 고객에게 안내문을 전달하고 해당되는 로트를 교환할 예정이다. 이와 관련 국내에서 발생한 사례는 없다는 것이다.
소비자는 제품에 표시된 고객센터에 문의 또는 구매처에 반품하면 된다.
 |
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

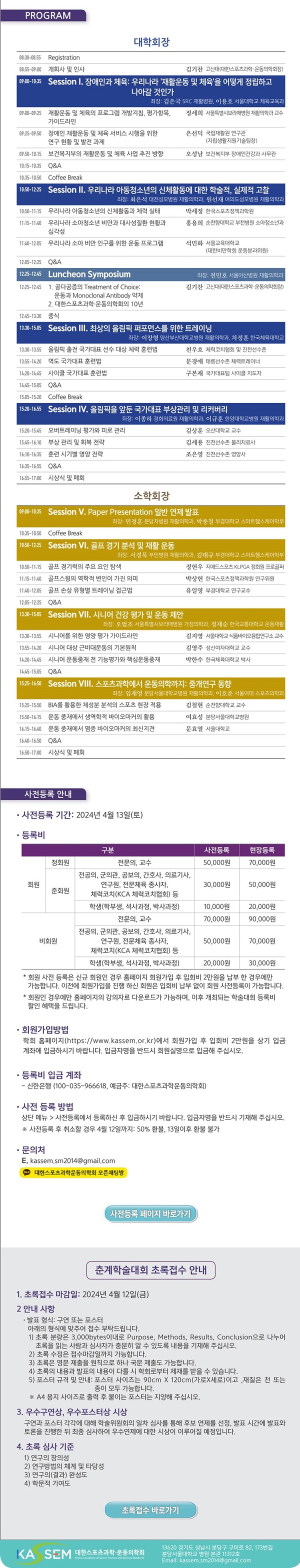 대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
