 |
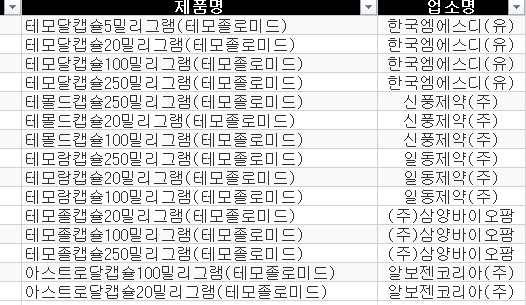
| ▲테모졸로미드 성분제제 |
일동제약(주) '테모람캡슐250mg', 삼양바이오팜 '테모졸캡슐20mg' 등 테모졸로미드제제의 이상반응 치명적인 패혈증 허가사항 추가 보고됐다.
식약처는 '테모졸로미드'성분제제의 美FDA 안전성 정보와 관련 국내·외 허가 현황, 제출의견 등 종합 검토한 결과에 따라 허가사항 변경지시 할 계획이며 오는 4월12일까지 사전예고한다고 밝혔다.
테모졸로미드 성분제제(분무제) 허가사항 변경대비표에 따르면 치명적인 결과 나타낸 사례를 포함한 패혈증이 보고됐다고 경고헸다.
또 이 약을 포함한 치료 방법으로 치료받던 환자들 중 매우 드물게 MDS 및 2차적 종양(골수성 백혈병 포함)이 보고된 바 있다.
재생불량성 빈혈을 유발할 수 있는 지속성 범혈구감소증이 보고됐으며 몇몇의 경우는 치명적인 결과를 나타냈다.
그리고 요붕증이 보고된 것을 비롯 독성 표피괴사용해와 스티븐스-존슨 증후군 사례가 매우 드물게 발현 보고됐다.
치명적인 결과를 나타낸 사례를 포함한 단순 헤르페스 뇌염이 보고됐다.
또 간질성 폐렴, 폐렴, 폐섬유증 및 치명적인 호흡부전이 매우 드물게 보고됐으며 간 효소의 증가, 고빌리루빈혈증, 담즙정체, 간염을 포함한 간독성이 확인됐다.
치명적인 간기능 상실을 비롯한 간손상이, 거대세포바이러스 감염과 거대세포바이러스와 B형 간염과 같은 감염의 재활성화가 보고됐다.
해당품목은 한국엠에스디(유) '테모달캡슐5mg', '테모달캡슐20mg', '테모달캡슐100mg', '테모달캡슐250mg', 신풍제약(주) '테몰드캡슐250mg', '테몰드캡슐20mg', '테몰드캡슐100mg', 일동제약(주) '테모람캡슐250mg', '테모람캡슐20mg', '테모람캡슐100mg', (주)삼양바이오팜 '테모졸캡슐20mg', '테모졸캡슐100mg', 테모졸캡슐250m, 알보젠코리아(주), '아스트로달캡슐100mg', '아스트로달캡슐20mg' 등 15품목이다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 동성제약, 쿠웨이트 수출 계약 체결...비건 새치 염색약 ‘허브’진출
동성제약, 쿠웨이트 수출 계약 체결...비건 새치 염색약 ‘허브’진출
