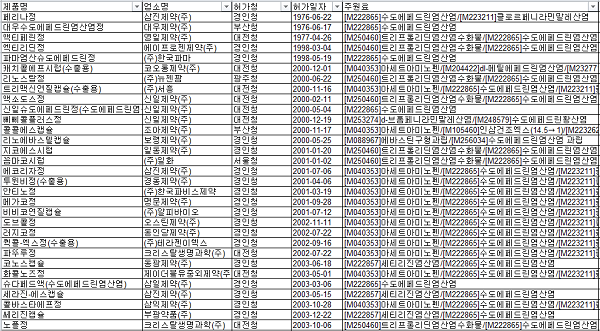
삼진제약(주) '세라진-에스캡슐' 등 '세티리진+슈도에페드린' 19품목,'아나필락시스성 쇼크'-'안통'-'발기기능장애’등 보고
삼일제약(주) '슈다페드액' 등 슈도에페드린제제 38품목에서 이상반응 '허혈성 대장염'이 추가 보고됐다.
또 삼진제약(주) '세라진-에스캡슐' 등 '세티리진+슈도에페드린' 19품목에서 이상반응 '아나필락시스성 쇼크', '조절장애', '시야흐림', '안통', '시각장애', '눈부심', '동공확대', '발기기능장애’등이 보고됐다.
식약처는 이같은 '슈도에페드린'함유제제의 유럽 의약품청(EMA) 안전성 정보와 관련 허가사항 변경지시 할 계획이며 이를 10월3일까지 사전예고한다고 18일 밝혔다.
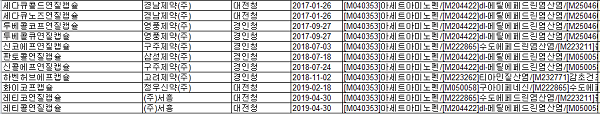
대우수도에페드린염산염정, 액티피드정, 코푸레스정, 하디코정, 뿌레콜에프캡슐, 캐치콜에프시럽 등 슈도에페드린 함유제제 허가사항 변경지시(안)에 따르면 이상반응 '허혈성 대장염'이 추가 보고됐다.
또 슈도에페드린 성분과 관련 허혈성 대장염의 증상 '급격한 복통, 직장 출혈 등'이 발현될 수 있어 이 약의 복용을 중단해야 한다는 일반적 주의사항이 신설됐다.
다만‘아세트아미노펜/슈도에페드린염산염/덱스트로메토르판브롬화수소산염수화물/클로르페니라민말레인산염’ 및 ‘염산펙소페나딘/염산슈도에페드린’ 성분제제는 해당 내용 기반영 및 통일조정 예정이므로 대상에서 제외됐다.
또한 '세티리진/슈도에페드린' 국외안전성 정보 및 슈도에페트린 국외안전성 정보에 따라
이상반응 '아나필락시스성 쇼크', '조절장애', '시야흐림', '안통', '시각장애', '눈부심', '동공확대', '발기기능장애’등 보고됐다.
 |
 |
 |
 |
 |
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

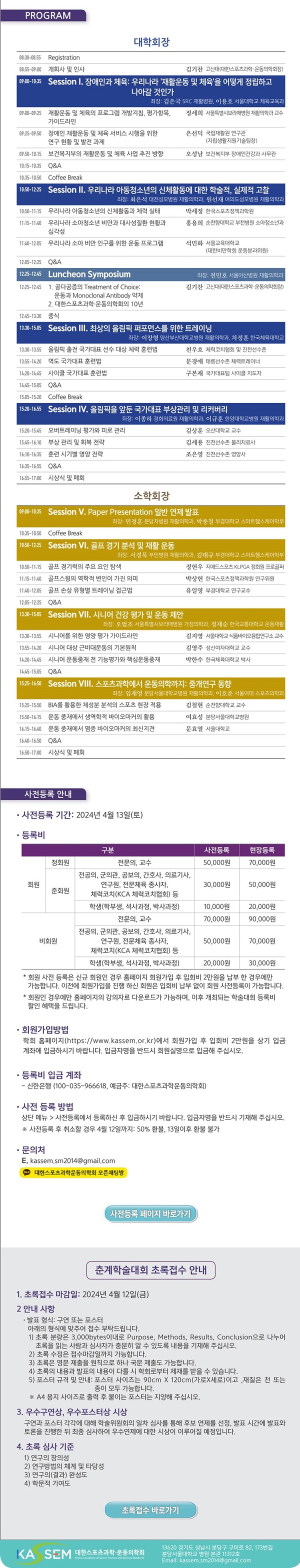 대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
대한스포츠과학·운동의학회, 오는 27일 ‘2024년 춘계학술대회’ 개최
