 |
 |
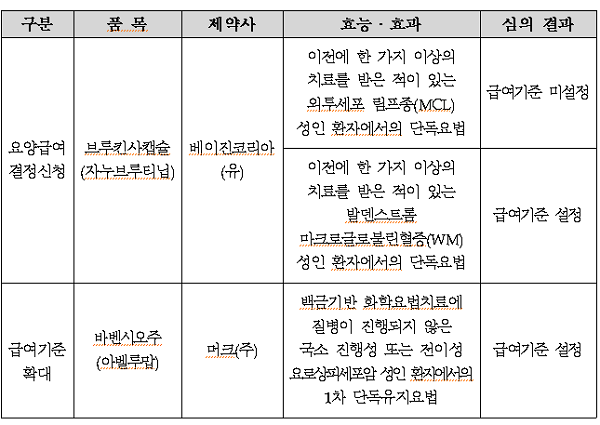
암 치료제 급여 기준 확대를 신청한 다국적 제약사들이 일부 품목은 '급여기준이 설정'된 반면 또다른 품목은 '미설정'이란 심의결과를 받아들이며 희비가 엇갈리고 있다.
지난 6일 끝난 2022년 제4차 암질환심의위원회에서 심의한 ‘암환자에게 사용되는 약제에 대한 급여기준 심의결과’에 따르면 요로상피세포암 1차 단독치료약 머크(주)의 '바벤시오주'는 급여기준 확대를 요청해 기준이 설정됐다. 이에 따라 백금기반 화학요법치료에 질병이 진행되지 않은 국소 진행성 또는 전이성 요로상피세포암 성인환자에 1차 요법에 사용될 전망이다.
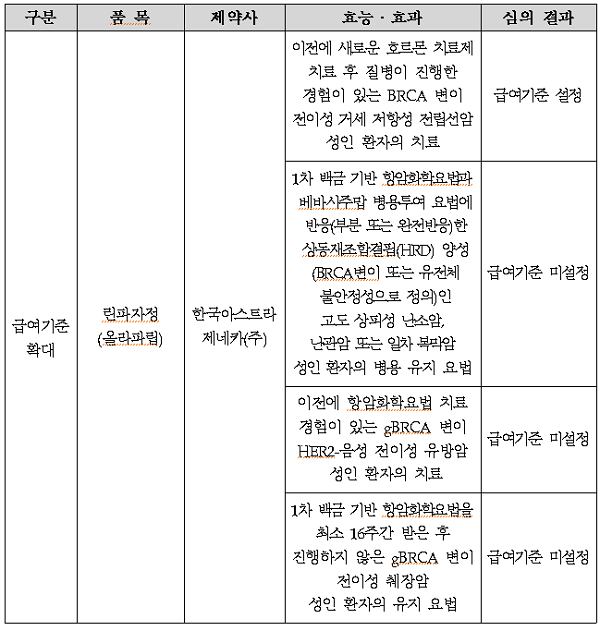
이전 새호르몬 치료제 치료 후 질병이 진행한 경험이 있는 BRCA 변이 전이성 거세 저항성 전립선암 성인 환자의 치료에 급여 기준이 설정된 한국아스트라제네카(주)의 '린파자정'은 1차 백금 기반 항암화학요법과 베바시주맙 병용투여 요법에 반응한 상동재조합결핍(HRD) 양성인 고도 상피성 난소암, 난관암, 1차 복막암 성인 환자의 병용 요법에 대해 급여가 승인되지 못했다.
또 이전에 항암화학요법 치료 경험이 있는 gBRCA 변이 HER2-음성 전이성 유방암 치료와 1차 백금 기반 항암화학요법을 최소 16주간 받은 후 진행하지 않은 gBRCA 변이 전이성 췌장암 성인 환자 유지 요법에도 급여 기준이 설정되지 못했다.
한정렬 기자 jrh05@hanmail.net
<저작권자 © 데일리메디팜, 무단 전재 및 재배포 금지>

 한국한의약진흥원, 한의약 산업 전문가 양성에 나선다
한국한의약진흥원, 한의약 산업 전문가 양성에 나선다
